标签: am
AAT代理,钙黄绿素蓝,AM
钙黄绿素蓝,AM
AAT代理,钙黄绿素蓝,AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素,AM,超级纯,
钙黄绿素,AM,超级纯,
AAT代理,钙黄绿素,AM,超级纯,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素,AM,超级纯,
钙黄绿素,AM,超级纯,
AAT代理,钙黄绿素,AM,超级纯,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素,AM
钙黄绿素,AM
AAT代理,钙黄绿素,AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,NAADP-AM
NAADP-AM
AAT代理,NAADP-AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,EDTA,AM酯
EDTA,AM酯
AAT代理,EDTA,AM酯,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,EDTA,AM酯
EDTA,AM酯
AAT代理,EDTA,AM酯,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,OG488 BAPTA-1,AM [相当于OregonGreen®488 BAPTA-1,AM] *渗透性*
OG488 BAPTA-1,AM [相当于OregonGreen®488 BAPTA-1,AM] *渗透性*
AAT代理,OG488 BAPTA-1,AM [相当于OregonGreen®488 BAPTA-1,AM] *渗透性*,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *
Fluo-4 AM *超纯级* * CAS 273221-67-3 *
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *
Fluo-4 AM *超纯级* * CAS 273221-67-3 *
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *
Fluo-4 AM *超纯级* * CAS 273221-67-3 *
AAT代理,Fluo-4 AM *超纯级* * CAS 273221-67-3 *,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,NAADP-AM
NAADP-AM
AAT代理,NAADP-AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素UltraGreenTM AM
钙黄绿素UltraGreenTM AM
AAT代理,钙黄绿素UltraGreenTM AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素UltraBlueTM AM
钙黄绿素UltraBlueTM AM
AAT代理,钙黄绿素UltraBlueTM AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素·深红(AM形式)
钙黄绿素·深红(AM形式)
AAT代理,钙黄绿素·深红(AM形式),微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,NAADP-AM(烟酸腺嘌呤二核苷酸磷酸)
NAADP-AM(烟酸腺嘌呤二核苷酸磷酸)
AAT代理,NAADP-AM(烟酸腺嘌呤二核苷酸磷酸),微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Cal Green 1,AM【替代Calcium Green-1,AM】
Cal Green 1,AM【替代Calcium Green-1,AM】
AAT代理,Cal Green 1,AM【替代Calcium Green-1,AM】,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fura-FF,AM【Fura-2FF,AM】,CAS:348079-12-9,
Fura-FF,AM【Fura-2FF,AM】,CAS:348079-12-9,
AAT代理,Fura-FF,AM【Fura-2FF,AM】,CAS:348079-12-9,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙黄绿素红,AM
钙黄绿素红,AM
AAT代理,钙黄绿素红,AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fura-8,AM【也称Fura-6】
Fura-8,AM【也称Fura-6】
AAT代理,Fura-8,AM【也称Fura-6】,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,Fura-8,AM【也称Fura-6】
Fura-8,AM【也称Fura-6】
AAT代理,Fura-8,AM【也称Fura-6】,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,BTC,AM
BTC,AM
AAT代理,BTC,AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙离子荧光探针Rhod-2,AM,超级纯,,大包装,
钙离子荧光探针Rhod-2,AM,超级纯,,大包装,
AAT代理,钙离子荧光探针Rhod-2,AM,超级纯,,大包装,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙螯合剂BAPTA,AM,超级纯,
钙螯合剂BAPTA,AM,超级纯,
AAT代理,钙螯合剂BAPTA,AM,超级纯,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,钙螯合剂BAPTA,AM
钙螯合剂BAPTA,AM
AAT代理,钙螯合剂BAPTA,AM,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
AAT代理,5-TAMRA,SE【5-羧基四甲基罗丹明,琥珀酰亚胺酯】,单体,
5-TAMRA,SE【5-羧基四甲基罗丹明,琥珀酰亚胺酯】,单体,
AAT代理,5-TAMRA,SE【5-羧基四甲基罗丹明,琥珀酰亚胺酯】,单体,,微信同号 18301939375,部分现货,欢迎来电咨询
上海金畔生物科技有限公司代理AAT Bioquest荧光染料全线产品,欢迎访问AAT Bioquest荧光染料官网了解更多信息。
Lab-TekTMⅡ腔室玻片,已灭菌,通过CE认证,孔数,1Nunc™Lab-Tek™IIChamberSlide™腔室载玻片系统154453,赛默Thermo代理
Lab-TekTMⅡ腔室玻片,已灭菌,通过CE认证,孔数,1 Nunc™ Lab-Tek™ II Chamber Slide™ 腔室载玻片系统
- 2008.00-12046.27
目录价:
- 154453
货号
- Nunc
品牌
- CCP
产品线
选择其它规格
| 名称 | 货号 | 品牌 | 规格 | 价格 | 购买 |
|---|
| Lab-TekTMⅡ腔室玻片,已灭菌,通过CE认证,孔数,8 | 154534 | Nunc | 96个/箱、16个/盒 | 联系微信:18301939375 |
| Lab-TekTMⅡ腔室玻片,已灭菌,通过CE认证,孔数,4 | 154526 | Nunc | 96个/箱、16片/盒 | 联系微信:18301939375 |
| Lab-TekTMⅡ腔室玻片,已灭菌,通过CE认证,孔数,2 | 154461 | Nunc | 96个/箱、16片/盒 | 联系微信:18301939375 |
- 商品详情
| 消毒 | Sterile |
|---|---|
| 培养面积 | 8.6cm2 |
| 描述 | 1-well Chamber Slide w/ removable well |
| 工作容积(公制) | 2.0 to 4.5mL |
| 孔 | 1 |
| 表面处理 | Cell Culture |
| 材料 | RS Glass |
| 物品描述 | Rectangular shape (74x25mm), clear polystyrene lid with handles on the top and side for aseptic manipulations |
| 每包 数量 | 16 |
| Unit Size | Case of 96 |
Thermo Scientific™ Nunc™ Lab-Tek™ II Chamber Slide™ 直接用于细胞培养、染色和观察,它包含一个可拆卸的聚苯乙烯培养腔室,该腔室与一个标准玻璃载玻片相连。载玻片表面经特殊处理,适用于贴壁细胞培养。1 孔、2 孔、4 孔和 8 孔形式可选。
●载玻片表面经特殊的 RS 冲洗处理,以确保细胞生长的一致性。
●带标签的聚苯乙烯盖允许气体交换,并能最大限度减少蒸发。
●拆卸工具可将培养腔室与载玻片分离。
●载玻片上印有生物兼容的粘性、疏水性孔边框。
●载玻片具有白色磨砂书写区。
。Thermo Scientific能够为客户提供一整套包括高端分析仪器、实验室装备、软件、服务、耗材和试剂在内的实验室综合解决方案。Fisher Scientific为卫生保健,科学研究,以及安全和教育领域的客户提供一系列的实验室装备、化学药品以及其他用品和服务。Thermo Fisher Scientific将努力为客户提供最为便捷的采购方案,为科研的飞速发展不断地改进工艺技术,提升客户价值,帮助股东提高收益,为员工创造良好的发展空间。
Amino-EG6-undecanethiol, hydrochloride试剂货号:A483
C23SH50ClNO6S
504.16
Rhod 2-AM试剂货号:R002
C52H59ClN4O19
1079.49
特点:
● 激发光557nm,发射光581nm
● 红色荧光与罗丹明相似
● 定位准确,信号强度高

产品性状
规格
性状 : 本产品为暗紫色固体,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图 : 符合实验要求
NMR光谱图 : 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
在所有的钙离子指示剂中,Rhod 2荧光信号的波长最长。它具有和罗丹明类似的激发和发射波长,分别为557 nm和581 nm。这样的激发波长使得我们很容易就能找到氩和氪光源的激光。尽管有人认为Rhod 2的荧光信号仅仅将钙复合物的荧光增加了数倍,但是Dojindo的Rhod 2由于具有很高的纯度,能有效地将钙荧光信号增加80-100倍左右,使得它的信号强度在所有的钙离子探针里面是最强的。所以,我们强烈建议使用Rhod 2作为探针用激光显微镜来检测细胞内的钙离子情况。有报道称,特别是在神经组织切片培养方面Rhod 2具有定位点的轮廓线更加清晰的特点。Rhod 2和钙离子的解离常数为(Kd=1.0 mM),在所有的钙离子荧光探针中是最高的,为监测钙离子浓度提供了一个广阔的范围。Rhod 2-AM是一种Rhod 2的乙酰甲酯衍生物,能非常容易的通过AM法负载到细胞内。
原理
与其他探针一样,Rhod 2-AM是将四个羧基全部作为脂溶性乙基甲酯体的细胞膜透明性物质。可以很容易地被细胞吸收。通过细胞内的脂肪酶水解成为Rhod 2,可以检测细胞内Ca2+。
激发发射波长
E x :557 nm
Em: 581 nm
溶解比例
溶解比例:1mg/ml(DMSO),50mg/ml(三氯甲烷)
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液 DMSO 需要保证新鲜无水,否则将会导致 AM 体水解,荧光染料无法进入细胞影响实验效果。
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成 5 μl/管,用封口膜封口,
并用铝箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
参考文献
1) R. Y. Tsien, “New Calcium Indicators and Buffers with High Selectivity against Magnesium and Protons: Design, Synthesis, and Properties of Prototype Structures”, Biochemistry, 1980, 19 (11), 2396.
2) R. Y. Tsien, T. Pozzan and T. J. Rink, “Calcium Homeostasis in Intact Lymphocytes: Cytoplasmic Free Calcium Monitored with a New, Intracellularly Trapped Fluorescent Indicator”, J. Cell Biol., 1982, 94, 325.
3) M. B. Feinstein, J. J. Egan, R. I. Sha’afi and J. White, “The Cytoplasmic Concentration of Free Calcium Inplatelets Is Controlled by Stimulators of Cyclic AMP Production (PGD2, PGE1, FORSKOLIN)”, Biochem. Biophys. Res. Commun., 1983, 113, 598.
4) N. Miyoshi, K. Hara, S. Kimura, K. Nakanishi and M. Fukuda, “A New Method of Determining Intracellular Free Ca2+ Concentration Using Quin 2-fluorescence”, Photochem. Photobiol., 1991, 53 (3), 415.
Q&A
|
Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
|
A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的 有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fluo 4-AM试剂货号:F311
C51H50F2N2O23
1096.94
特点:
● 激发波长494 nm,发射波长516 nm
● 激光共聚焦,流式细胞仪均可检测
● 荧光强度高
产品性状
规格
性状 : 本产品为橙红色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图: 符合实验要求
NMR光谱图: 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
Fluo 4是一种将Fluo 3结构中的Cl替换成F的钙荧光探针。由于将Cl替换成了电子吸引力更强的F,它的最大激发波长会向短波长处偏离10 nm左右。这个波长更接近于氩激光器的波长,所以用氩激光器激发时,Fluo 4的荧光强度比Fluo 3强1倍。
原理
Fluo 4-AM是一种可以穿透细胞膜的荧光染料,需用无水DMSO配制。Fluo 4-AM进入细胞后可以被细胞内的酯酶剪切形成Fluo 4,从而被滞留在细胞内。产生的Fluo 4随后会和钙离子(Ca2+)结合并发出荧光。由于Fluo 4与钙离子的亲和力和Fluo 3近似(Fluo 3:Kd=0.4 μmol/l、Fluo 4: Kd=0.36 μmol/l),所以使用上和Fluo 3也基本相同,可以使用激光共聚焦显微镜或流式细胞仪等仪器检测细胞内钙离子浓度的变化。钙离子探针种类繁多,根据不同的实验要求,选择不同的产品。
激发发射波长
E x :494 nm
E m :516 nm
操作步骤
1、用 HBSS 溶液稀释 1-5 mmol/l 的 Fluo 4-AM 母液,配制成 1-5 µmol/l 的 Fluo 4-AM 工作液。
(此浓度仅供参考,请根据具体实验要求自行调整)
例如:1 mmol/l 母液配制 1 ml 浓度为 5 µmol/l 工作液的方法:用 1 ml HBSS 溶液稀释 5 µl 母
液即可。Fluo 4-AM 工作液需要即配即用,请勿反复冻存。如果Fluo 4-AM进入细胞的效果不好,可
使用Pluronic® F-127,后者可以防止Fluo 4-AM在缓冲液里聚合并能促进其进入细胞。
*Pluronic® F-127 先用DMSO溶解至浓度为 20%(W/V),然后根据实验需要直接加入Fluo 4-AM工作
液中至终浓度为 0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,使用 HBSS 溶液洗涤细胞 3 次。如果使用含血清的培养基,血清中
的酯酶会分解 AM 体,从而降低 Fluo 4-AM 进入细胞的效果。另外含有酚红的培养基会使本底值略
微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入 Fluo 4-AM 工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育 10-60 分钟,除去 Fluo 4-AM 工作液。关于孵育的时间,如果首次做实验不能
确定,建议先孵育 30 分钟,看荧光效果:如果细胞死亡较多,适当缩短时间;如果荧光强度太
弱,适当延长时间。
5、用 HBSS溶液洗涤细胞 3 次,以充分去除残留的 Fluo 4-AM 工作液。然后加入 HBSS 溶液覆盖细胞。
6、37℃培养箱孵育约 20-30 分钟,以确保 AM 体在细胞内的完全去酯化作用。
如果细胞内酯酶活性较低,建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用激光共聚焦或荧光显微镜检测细胞,激发波长 494 nm,发射波长 516 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致 AM 体水解,使荧光染料无法进入细胞,影响实验效果
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成 5 μl/管,用封口膜封口,
并用铝箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
数据处理
计算公式:
[Ca2+]i = Kd×(F-Fmin) / (Fmax-F)
[Ca2+]i :细胞内Ca2+浓度
Kd:解离常数
F :荧光强度
Fmin:Ca2+为零状态下测得的荧光比值
Fmax:Ca2+为饱和状态下测得的荧光比值
文献
1) A. Minta, J. P. Y. Kao and R. Y. Tsien, “Fluorescent Indicators for Cytosolic Calcium Based on Rhodamine and Fluorescein Chromophores”, J. Biol. Chem., 1989, 264(14), 8171.
2) J. P. Kao, A. T. Harootunian and R. Y. Tsien, “Photochemically Generated Cytosolic Calcium Pulses and Their Detection by Fluo-3”, J. Biol. Chem., 1989, 264, 8179.
3) M. Eberhard and P. Erne, “Kinetics of Calcium Binding to Fluo-3 by Stopped-Flow Fluorescence”, Biochem. Biophys. Res. Commun., 1989, 163, 309.
4) A. Hernandez-Cruz, F. Sala and P. R. Adams, “Subcellular Calcium Transients Visualized by Confocal Microscopy in a Voltage-clamped Vertebrate Neuron”, Science, 1990, 247, 858.
5) A. H. Cornell-Bell, S. M. Finkbeiner, M. S. Cooper and S. J. Smith, “Glutamate Induces Calcium Waves in Cultured Astrocytes: Long-Range Glial Signaling”, Science, 1990, 247, 470.
6) D. A. Williams, “Quantitative Intracellular Calcium Imaging with Laser-scanning Confocal Microscopy”, Cell Calcium, 1990, 11, 589.
7) D. A. Williams, S. H. Cody, C. A. Gehring, R. W. Parish and P. J. Harris, “Confocal Imaging of Ionised Calcium in Living Plant Cells”, Cell Calcium, 1990, 11, 291.
8) P. A. Vandenberghe and J. L. Ceuppens, “Flow Cytometric Measurement of Cytoplasmic Free Calcium in Human Peripheral Blood T Lymphocytes with Fluo-3, A New Fluorescent Calcium Indicator”, J. Immunol. Methods, 1990, 127, 197.
10) M. Iino, H. Kasai and T. Yamazawa, “Visualization of Neural Control of Intracellular Ca2+ Concentration in Single Vascular Smooth Muscle Cells in situ”, EMBO J., 1994, 13 (21), 5026.
11) M. E. Dailey and S. J. Smith, “Spontaneous Ca2+ Transients in Developing Hippocampal Pyramidal Cells”, J. Neurobiol., 1994, 25(3), 243.
12) M. Burnier, G. Centeno, E. Burki and H. R. Brunner, “Confocal Microscopy to Analyze Cytosolic and Nuclear Calcium in Cultured Vascular Cells”, Am. J. Physiol., 1994, 266, C1118.
13) E. Donnadieu and L. Y. W. Bourguignon, “Ca2+ Signaling in Endothelial Cells Stimulated by Bradykinin: Ca2+ Measurement in the Mitochondria and the Cytosol by Confocal Microscopy”, Cell Calcium, 1996, 20 (1), 53.
14) M. Ikeda, H. Ariyoshi, J. Kambayashi, K. Fujitani, N. Shinoki, M. Sakon, T. Kawasaki and M. Monden, “Separate Analysis of Nuclear and Cytosolic Ca2+ Concentrations in Human Umbilical Vein Endothelial Cells”, J. Cell. Biochem., 1996, 63 (1), 23.
15) J. E. Merritt, S. A. McCarthy, M. P. A. Davies and K. E. Moores, “Use of fluo-3 to Measure Cytosolic Ca2+ in Platelets and Neutrophils Loading Cells with the Dye, Calibration of Traces, Measurements in the Presence of Plasma, and Buffering of Cytosolic Ca2+”, Biochem. J., 1990, 269, 513.
Q&A
|
Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
|
A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的 有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fluo 4-AM special packaging试剂货号:F312
C51H50F2N2O23
1096.94
特点:
● 激发波长494 nm,发射波长516 nm
● 激光共聚焦,流式细胞仪均可检测
● 荧光强度高

凑单关联产品TOP5
NO.1. Annexin V, FITC Apoptosis Detection Kit 细胞凋亡检测
NO.2. BCECF-AM 细胞内pH值检测
NO.3. Calcein-AM/PI Double Staining Kit 活死细胞双染
NO.4. Cell Counting Kit-8 细胞增殖毒性检测
NO.5. Cytotoxicity LDH Assay Kit-WST 乳酸脱氢酶(LDH)检测
产品性状
规格
性状 : 本产品为橙红色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图 : 符合实验要求
NMR光谱图 : 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
Fluo 4是一种将Fluo 3结构中的Cl替换成F的钙荧光探针。由于将Cl替换成了电子吸引力更强的F,它的最大激发波长会向短波长处偏离10 nm左右。这个波长更接近于氩激光器的波长,所以用氩激光器激发时,Fluo 4的荧光强度比Fluo 3强1倍。
原理
Fluo 4-AM是一种可以穿透细胞膜的荧光染料,需用无水DMSO配制。Fluo 4-AM进入细胞后可以被细胞内的酯酶剪切形成Fluo 4,从而被滞留在细胞内。产生的Fluo 4随后会和钙离子(Ca2+)结合并发出荧光。由于Fluo 4与钙离子的亲和力和Fluo 3近似(Fluo 3:Kd=0.4 μmol/l、Fluo 4: Kd=0.36 μmol/l),所以使用上和Fluo 3也基本相同,可以使用激光共聚焦显微镜或流式细胞仪等仪器检测细胞内钙离子浓度的变化。钙离子探针种类繁多,根据不同的实验要求,选择不同的产品。
激发发射波长
E x :494 nm
E m :516 nm
操作步骤
1、用 HBSS 溶液稀释 1-5 mmol/l 的 Fluo 4-AM 母液,配制成 1-5 µmol/l 的 Fluo 4-AM 工作液。
(此浓度仅供参考,请根据具体实验要求自行调整)
例如:1 mmol/l 母液配制 1 ml 浓度为 5 µmol/l 工作液的方法:用 1 ml HBSS 溶液稀释 5 µl 母
液即可。Fluo 4-AM 工作液需要即配即用,请勿反复冻存。如果Fluo 4-AM进入细胞的效果不好,可
使用Pluronic® F-127,后者可以防止Fluo 4-AM在缓冲液里聚合并能促进其进入细胞。
*Pluronic® F-127 先用DMSO溶解至浓度为 20%(W/V),然后根据实验需要直接加入Fluo 4-AM工作
液中至终浓度为 0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,使用 HBSS 溶液洗涤细胞 3 次。如果使用含血清的培养基,血清中
的酯酶会分解 AM 体,从而降低 Fluo 4-AM 进入细胞的效果。另外含有酚红的培养基会使本底值略
微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入 Fluo 4-AM 工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育 10-60 分钟,除去 Fluo 4-AM 工作液。关于孵育的时间,如果首次做实验不能
确定,建议先孵育30分钟看荧光效果:如果细胞死亡较多,适当缩短时间;如果荧光强度太弱,
适当延长时间。
5、用 HBSS溶液洗涤细胞 3 次,以充分去除残留的 Fluo 4-AM 工作液。然后加入 HBSS 溶液覆盖细胞。
6、37℃培养箱孵育约 20-30 分钟,以确保 AM 体在细胞内的完全去酯化作用。
如果细胞内酯酶活性较低,建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用激光共聚焦或荧光显微镜检测细胞,激发波长 494 nm,发射波长 516 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致 AM 体水解,使荧光染料无法进入细胞,影响实验效果
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成 5 μl/管,用封口膜封口,
并用铝箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
数据处理
计算公式:
[Ca2+]i = Kd×(F-Fmin) / (Fmax-F)
[Ca2+]i :细胞内Ca2+浓度
Kd:解离常数
F :荧光强度
Fmin:Ca2+为零状态下测得的荧光比值
Fmax:Ca2+为饱和状态下测得的荧光比值
文献
1) A. Minta, J. P. Y. Kao and R. Y. Tsien, “Fluorescent Indicators for Cytosolic Calcium Based on Rhodamine and Fluorescein Chromophores”, J. Biol. Chem., 1989, 264(14), 8171.
2) J. P. Kao, A. T. Harootunian and R. Y. Tsien, “Photochemically Generated Cytosolic Calcium Pulses and Their Detection by Fluo-3”, J. Biol. Chem., 1989, 264, 8179.
3) M. Eberhard and P. Erne, “Kinetics of Calcium Binding to Fluo-3 by Stopped-Flow Fluorescence”, Biochem. Biophys. Res. Commun., 1989, 163, 309.
4) A. Hernandez-Cruz, F. Sala and P. R. Adams, “Subcellular Calcium Transients Visualized by Confocal Microscopy in a Voltage-clamped Vertebrate Neuron”, Science, 1990, 247, 858.
5) A. H. Cornell-Bell, S. M. Finkbeiner, M. S. Cooper and S. J. Smith, “Glutamate Induces Calcium Waves in Cultured Astrocytes: Long-Range Glial Signaling”, Science, 1990, 247, 470.
6) D. A. Williams, “Quantitative Intracellular Calcium Imaging with Laser-scanning Confocal Microscopy”, Cell Calcium, 1990, 11, 589.
7) D. A. Williams, S. H. Cody, C. A. Gehring, R. W. Parish and P. J. Harris, “Confocal Imaging of Ionised Calcium in Living Plant Cells”, Cell Calcium, 1990, 11, 291.
8) P. A. Vandenberghe and J. L. Ceuppens, “Flow Cytometric Measurement of Cytoplasmic Free Calcium in Human Peripheral Blood T Lymphocytes with Fluo-3, A New Fluorescent Calcium Indicator”, J. Immunol. Methods, 1990, 127, 197.
10) M. Iino, H. Kasai and T. Yamazawa, “Visualization of Neural Control of Intracellular Ca2+ Concentration in Single Vascular Smooth Muscle Cells in situ”, EMBO J., 1994, 13 (21), 5026.
11) M. E. Dailey and S. J. Smith, “Spontaneous Ca2+ Transients in Developing Hippocampal Pyramidal Cells”, J. Neurobiol., 1994, 25(3), 243.
12) M. Burnier, G. Centeno, E. Burki and H. R. Brunner, “Confocal Microscopy to Analyze Cytosolic and Nuclear Calcium in Cultured Vascular Cells”, Am. J. Physiol., 1994, 266, C1118.
13) E. Donnadieu and L. Y. W. Bourguignon, “Ca2+ Signaling in Endothelial Cells Stimulated by Bradykinin: Ca2+ Measurement in the Mitochondria and the Cytosol by Confocal Microscopy”, Cell Calcium, 1996, 20 (1), 53.
14) M. Ikeda, H. Ariyoshi, J. Kambayashi, K. Fujitani, N. Shinoki, M. Sakon, T. Kawasaki and M. Monden, “Separate Analysis of Nuclear and Cytosolic Ca2+ Concentrations in Human Umbilical Vein Endothelial Cells”, J. Cell. Biochem., 1996, 63 (1), 23.
15) J. E. Merritt, S. A. McCarthy, M. P. A. Davies and K. E. Moores, “Use of fluo-3 to Measure Cytosolic Ca2+ in Platelets and Neutrophils Loading Cells with the Dye, Calibration of Traces, Measurements in the Presence of Plasma, and Buffering of Cytosolic Ca2+”, Biochem. J., 1990, 269, 513.
Q&A
| Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
| A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的
有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fluo 3-AM试剂货号:F023
C51H50Cl2N2O23
1129.85
特点:
● 激发波长480-500 nm,发射波长523-530 nm
● 激光共聚焦,流式细胞仪均可检测

产品性状
规格
性状 : 本产品为红色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图: 符合实验要求
NMR光谱图: 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
Fluo 3-AM是一种检测细胞内钙离子的荧光探针。Fluo 3若以游离配体形式存在时几乎是非荧光性的,但是当它与钙离子Ca2+结合后荧光会增加60至80倍,是目前最常用的一种钙离子荧光探针。激光共聚焦荧光显微镜具有氩激光器,所以Fluo 3可被广泛使用于这种显微镜上。这种荧光信号发出来的长波也便于减小对样品细胞的光损伤。Fluo 3也可用来检测紫外光照射下可裂解的螯合钙或其它形式的钙。Fluo 3-AM是Fluo 3的一种乙酰甲酯衍生物,通过培养,能够轻易进入细胞中。
原理
Fluo 3-AM (钙离子荧光探针) 需用无水DMSO (anhydrous DMSO)配制。Fluo 3-AM是一种可以穿透细胞膜的荧光染料。Fluo 3-AM进入细胞后可以被细胞内的酯酶剪切形成Fluo 3,从而被滞留在细胞内。Fluo 3可以和钙离子结合,结合钙离子后可以产生较强的荧光,最大激发波长为506nm,最大发射波长为526nm
激发发射波长
E x :480-500 nm
E m :525-530 nm
操作步骤
1、用 HBSS 溶液稀释 1-5 mmol/l 的 Fluo 3-AM 母液,配制成 1-5 µmol/l的 Fluo 3-AM 工作液
(此浓度仅供参考,请根据具体实验要求自行调整)。
例如:1 mmol/l 母液配制 1 ml 浓度为 5 µmol/l工作液的方法:用 1 ml HBSS 溶液稀释 5 µl母液
即可。Fluo 3-AM 工作液需要即配即用,请勿反复冻存。如果Fluo 3-AM进入细胞的效果不好,
可使用Pluronic® F-127,后者可以防止Fluo 3-AM在缓冲液里聚合并能促进其进入细胞。
*Pluronic® F-127先用DMSO溶解至浓度为 20%(W/V),然后根据实验需要直接加入Fluo 3-AM工作液
中至终浓度为 0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,用 HBSS 溶液洗涤细胞 3 次。
如果使用含血清的培养基,血清中的酯酶会分解 AM 体,从而降低 Fluo 3-AM 进入细胞的效果。
另外含有酚红的培养基会使本底值略微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入 Fluo 3-AM 工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育10-60分钟,除去Fluo 3-AM工作液。关于孵育的时间,如果首次做实验不能定,
建议先孵育 30 分钟,看荧光效果:如果细胞死亡较多,适当缩短时间;如果荧光强度太弱,
适当延长时间。
5、用 HBSS 溶液洗涤细胞 3 次以充分去除残留的 Fluo 3-AM 工作液。然后加入 HBSS 溶液覆盖细胞。
6、37℃培养箱孵育约 20-30 分钟,以确保 AM 体在细胞内的完全去酯化作用。
如果细胞内酯酶活性较低,建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用激光共聚焦或荧光显微镜检测细胞,激发波长 480-500 nm,发射波长 525-530 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致AM体水解,使荧光染料无法进入细胞,影响实验效果。
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成5 μl/管,用封口膜封口,并用
铝箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针终浓度、培养时间等,找到最佳实验条件。
实验例
加载了Fluo 3的新鲜分离的大鼠肝脏细胞PE刺激后出现规则胞浆钙振荡。
上图为细胞明场图和不同时间点(min)的比例成像,
下图为影响Fluo 3荧光强度随时间的变化。
成像系统:Photon Technology International Inc.,
显微镜Nikon TE2000U,CCD相机QuantEM512S,软件ERP。
(北京师范大学细胞生物学研究所 崔宗杰教授 提供照片)
数据分析
计算公式:
[Ca2+]i = Kd×(F-Fmin) / (Fmax-F)
[Ca2+]i :细胞内Ca2+浓度
Kd:解离常数
F :荧光强度
Fmin:Ca2+为零状态下测得的荧光比值
Fmax:Ca2+为饱和状态下测得的荧光比值
Q&A
| Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
| A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的
有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fluo 3-AM试剂货号:F026
C51H50Cl2N2O23
1129.85
特点:
● 激发波长480-500 nm,发射波长523-530 nm
● 激光共聚焦,流式细胞仪均可检测

产品性状
规格
性状 : 本产品为红色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图: 符合实验要求
NMR光谱图: 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
Fluo 3-AM是一种检测细胞内钙离子的荧光探针。Fluo 3若以游离配体形式存在时几乎是非荧光性的,但是当它与钙离子Ca2+结合后荧光会增加60至80倍,是目前最常用的一种钙离子荧光探针。激光共聚焦荧光显微镜具有氩激光器,所以Fluo 3可被广泛使用于这种显微镜上。这种荧光信号发出来的长波也便于减小对样品细胞的光损伤。Fluo 3也可用来检测紫外光照射下可裂解的螯合钙或其它形式的钙。Fluo 3-AM是Fluo 3的一种乙酰甲酯衍生物,通过培养,能够轻易进入细胞中。
原理
Fluo 3-AM (钙离子荧光探针) 需用无水DMSO (anhydrous DMSO)配制。Fluo 3-AM是一种可以穿透细胞膜的荧光染料。Fluo 3-AM进入细胞后可以被细胞内的酯酶剪切形成Fluo 3,从而被滞留在细胞内。Fluo 3可以和钙离子结合,结合钙离子后可以产生较强的荧光,最大激发波长为506nm,最大发射波长为526nm
激发发射波长
E x :480-500 nm
Em:525-530 nm
操作步骤
1、用 HBSS 溶液稀释 1-5 mmol/l 的 Fluo 3-AM 母液,配制成 1-5 µmol/l的 Fluo 3-AM 工作液
(此浓度仅供参考,请根据具体实验要求自行调整)。
例如:1 mmol/l 母液配制 1 ml 浓度为 5 µmol/l工作液的方法:用 1 ml HBSS 溶液稀释 5 µl母液
即可。Fluo 3-AM 工作液需要即配即用,请勿反复冻存。如果Fluo 3-AM进入细胞的效果不好,
可使用Pluronic® F-127,后者可以防止Fluo 3-AM在缓冲液里聚合并能促进其进入细胞。
*Pluronic® F-127先用DMSO溶解至浓度为 20%(W/V),然后根据实验需要直接加入Fluo 3-AM工作液
中至终浓度为 0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,用 HBSS 溶液洗涤细胞 3 次。
如果使用含血清的培养基,血清中的酯酶会分解 AM 体,从而降低 Fluo 3-AM 进入细胞的效果。
另外含有酚红的培养基会使本底值略微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入 Fluo 3-AM 工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育10-60分钟,除去Fluo 3-AM工作液。关于孵育的时间,如果首次做实验不能定,
建议先孵育 30 分钟,看荧光效果:如果细胞死亡较多,适当缩短时间;如果荧光强度太弱,
适当延长时间。
5、用 HBSS 溶液洗涤细胞 3 次以充分去除残留的 Fluo 3-AM 工作液。然后加入 HBSS 溶液覆盖细胞。
6、37℃培养箱孵育约 20-30 分钟,以确保 AM 体在细胞内的完全去酯化作用。
如果细胞内酯酶活性较低,建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用激光共聚焦或荧光显微镜检测细胞,激发波长 480-500 nm,发射波长 525-530 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致AM体水解,荧光染料无法进入细胞,影响实验效果
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成5 μl/管,用封口膜封口,并用铝
箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
实验案例
加载了Fluo 3的新鲜分离的大鼠肝脏细胞PE刺激后出现规则胞浆钙振荡。
上图为细胞明场图和不同时间点(min)的比例成像,
下图为影响Fluo 3荧光强度随时间的变化。
成像系统:Photon Technology International Inc.,
显微镜Nikon TE2000U,CCD相机QuantEM512S,软件ERP。
(北京师范大学细胞生物学研究所 崔宗杰教授 提供照片)
数据分析
计算公式:
[Ca2+]i = Kd×(F-Fmin) / (Fmax-F)
[Ca2+]i :细胞内Ca2+浓度
Kd:解离常数
F :荧光强度
Fmin:Ca2+为零状态下测得的荧光比值
Fmax:Ca2+为饱和状态下测得的荧光比值
文献
1) A. Minta, J. P. Y. Kao and R. Y. Tsien, “Fluorescent Indicators for Cytosolic Calcium Based on Rhodamine and Fluorescein Chromophores”, J. Biol. Chem., 1989, 264(14), 8171.
2) J. P. Kao, A. T. Harootunian and R. Y. Tsien, “Photochemically Generated Cytosolic Calcium Pulses and Their Detection by Fluo-3”, J. Biol. Chem., 1989, 264, 8179.
3) M. Eberhard and P. Erne, “Kinetics of Calcium Binding to Fluo-3 by Stopped-Flow Fluorescence”, Biochem. Biophys. Res. Commun., 1989, 163, 309.
4) A. Hernandez-Cruz, F. Sala and P. R. Adams, “Subcellular Calcium Transients Visualized by Confocal Microscopy in a Voltage-clamped Vertebrate Neuron”, Science, 1990, 247, 858.
5) A. H. Cornell-Bell, S. M. Finkbeiner, M. S. Cooper and S. J. Smith, “Glutamate Induces Calcium Waves in Cultured Astrocytes: Long-Range Glial Signaling”, Science, 1990, 247, 470.
6) D. A. Williams, “Quantitative Intracellular Calcium Imaging with Laser-scanning Confocal Microscopy”, Cell Calcium, 1990, 11, 589.
7) D. A. Williams, S. H. Cody, C. A. Gehring, R. W. Parish and P. J. Harris, “Confocal Imaging of Ionised Calcium in Living Plant Cells”, Cell Calcium, 1990, 11, 291.
8) P. A. Vandenberghe and J. L. Ceuppens, “Flow Cytometric Measurement of Cytoplasmic Free Calcium in Human Peripheral Blood T Lymphocytes with Fluo-3, A New Fluorescent Calcium Indicator”, J. Immunol. Methods, 1990, 127, 197.
10) M. Iino, H. Kasai and T. Yamazawa, “Visualization of Neural Control of Intracellular Ca2+ Concentration in Single Vascular Smooth Muscle Cells in situ”, EMBO J., 1994, 13 (21), 5026.
11) M. E. Dailey and S. J. Smith, “Spontaneous Ca2+ Transients in Developing Hippocampal Pyramidal Cells”, J. Neurobiol., 1994, 25(3), 243.
12) M. Burnier, G. Centeno, E. Burki and H. R. Brunner, “Confocal Microscopy to Analyze Cytosolic and Nuclear Calcium in Cultured Vascular Cells”, Am. J. Physiol., 1994, 266, C1118.
13) E. Donnadieu and L. Y. W. Bourguignon, “Ca2+ Signaling in Endothelial Cells Stimulated by Bradykinin: Ca2+ Measurement in the Mitochondria and the Cytosol by Confocal Microscopy”, Cell Calcium, 1996, 20 (1), 53.
14) M. Ikeda, H. Ariyoshi, J. Kambayashi, K. Fujitani, N. Shinoki, M. Sakon, T. Kawasaki and M. Monden, “Separate Analysis of Nuclear and Cytosolic Ca2+ Concentrations in Human Umbilical Vein Endothelial Cells”, J. Cell. Biochem., 1996, 63 (1), 23.
15) J. E. Merritt, S. A. McCarthy, M. P. A. Davies and K. E. Moores, “Use of fluo-3 to Measure Cytosolic Ca2+ in Platelets and Neutrophils Loading Cells with the Dye, Calibration of Traces, Measurements in the Presence of Plasma, and Buffering of Cytosolic Ca2+”, Biochem. J., 1990, 269, 513.
Q&A
|
Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
|
A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的 有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fura2-AM special packaging试剂货号:F025
C44H47N3O24
1001.85
特点:
● 双波长激发检测钙离子
● 激光共聚焦,流式细胞仪均可检测
● 荧光强度高

产品性状
规格
性状 : 本产品为黄色或橙黄色粉末,使用时将固体溶解于无水DMSO中
纯度(HPLC): 98%以上
荧光光谱图: 符合实验要求
NMR光谱图: 符合实验要求
处理条件
保存方法 : 避光冷冻
产品概述
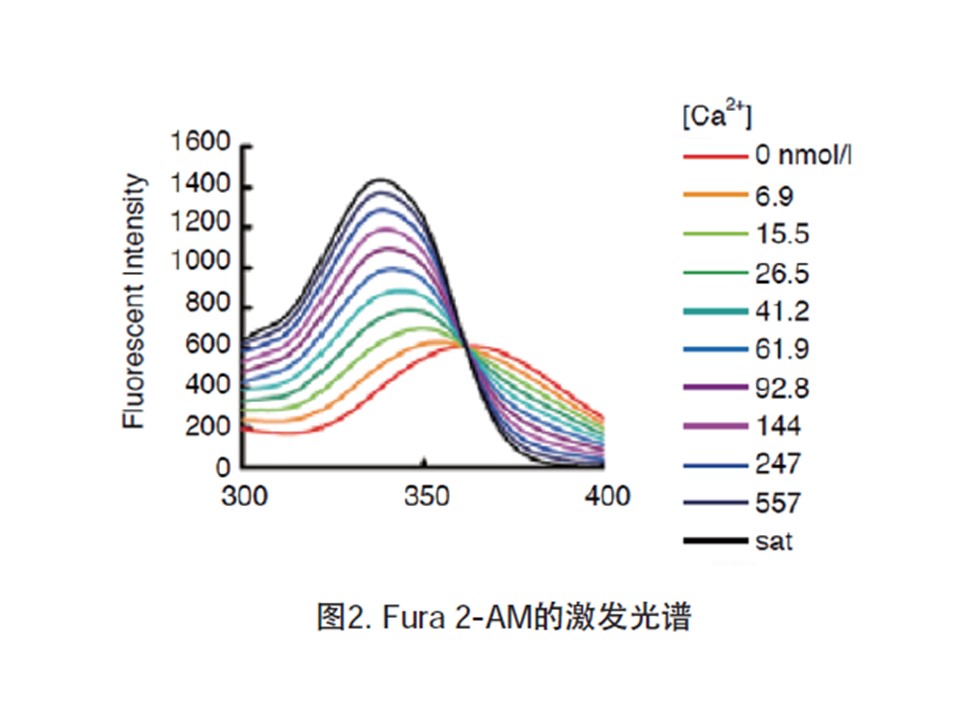
Fura 2-AM是一种可以穿透细胞膜的荧光染料。Fura 2-AM的荧光比较弱,最大激发波长为369 nm,最大发射波长为478 nm,并且其荧光不会随钙离子浓度改变而改变。Fura 2-AM进入细胞后可以被细胞内的酯酶剪切形成Fura 2,从而被滞留在细胞内。Fura 2和钙离子结合后,最大激发波长为335 nm(最大激发波长随离子浓度的的不同而有所不同),最大发射波长为505nm。实际检测时推荐使用的激发波长为340nm,发射波长为510 nm。如果做双波长检测,则推荐使用的激发波长为340 nm和380 nm。
原理
Fura 2可以和钙离子(Ca2+)结合,结合钙离子后在330-350 nm激发光下可以产生较强的荧光,而在380 nm激发光下则会导致荧光减弱。这样就可以使用340 nm和380 nm这两个荧光的比值来检测细胞内的钙离子浓度,可以消除不同细胞样品间荧光探针装载效率的差异,荧光探针的渗漏,细胞厚度差异等一些误差因素。
激发发射波长
Ex :340~380 nm
Em :510 nm

操作步骤
1、用HBSS溶液稀释1-5 mmol/l的Fura 2-AM母液,配制成1-5 μmol/l的Fura 2-AM工作液。
(此浓度仅供参考,请根据具体实验要求自行调整)
例如:1 mmol/l母液配制1 ml浓度为5 μmol/l工作液的方法:用1 ml HBSS溶液稀释5μl母液即可。
如果Fura 2-AM进入细胞的效果不好,可使用Pluronic® F-127,后者可以防止Fura 2-AM在缓冲液里
聚合并能促进其进入细胞。
*Pluronic® F-127先用DMSO溶解至浓度为20%(W/V),然后根据实验需要直接加入Fura 2-AM工作液
中至终浓度为0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,使用HBSS溶液洗涤细胞3次。
如果使用含血清的培养基,血清中的酯酶会分解AM体,从而降低Fura 2-AM进入细胞的效果。
另外含有酚红的培养 基会使本底值略微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入Fura 2-AM工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育10-60分钟,除去Fura 2-AM工作液。关于孵育的时间,如果首次做实验不能定
建议先孵育30分钟,看荧光效果:如果细胞死亡较多,缩短时间;荧光强度太弱,延长时间。
5、用HBSS溶液洗涤细胞3次,以充分去除残留的Fura 2-AM工作液。然后加入HBSS溶液覆盖细胞。
6、37℃培养箱孵育约20-30分钟,以确保AM体在细胞内的完全去酯化作用。如果细胞内酯酶活性较低,
建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用流式细胞仪或其它设备检测细胞,激发波长380 nm(Fura 2)和340 nm(钙离子-Fura 2),
发射波长510 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致AM体水解,使荧光染料无法进入细胞,影响实验效果。
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成5 μl/管,用封口膜封口,并用铝箔纸包裹,
放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件。
数据处理
Fλ1与Fλ2分别是λ1与λ2激发时的总荧光强度,Sf 1与Sf 2是两种紫外光激发时游离Fura-2 (未结合Ca2+)的荧光系数,
Cf是游离的Fura-2浓度,Sb1与Sb2是相应波长下结合Ca2+后Fura-2的荧光系数,Cb是结合Ca2+的Fura-2浓度
参考文献
1) G. Grynkiewicz, M. Poenie and R. Y. Tsien, “A New Generation of Ca2+ Indicators with Greatly Improved Fluorescence Properties”, J. Biol. Chem., 1985, 260, 3440.
2) D. A. Williams, K. E. Fogarty, R. Y. Tsien and F. S. Fay, “Calcium Gradients in Single Smooth Muscle Cells Revealed by the Digital Imaging Microscope Using Fura-2”, Nature, 1985, 318, 558.
3) R. Y. Tsien, T. J. Rink and M. Poenie, “Measurement of Cytosolic Free Ca2+ in Individual Small Cells Using Fluorescence Microscopy with Dual Excitation Wavelengths”, Cell Calcium, 1985, 6, 145.
4) D. A. Williams and F. S. Fay, “Intracellular Calibration of the Fluorescent Calcium Indicator Fura-2”, Cell Calcium, 1990, 11, 75.
5) W. Almers and E. Neher, “The Ca Signal from Fura-2 Loaded Mast Cells Depends Strongly on the Method of Dye-loading”, FEBS Lett., 1985, 192, 13.
6) G. H. R. Rao, J. D. Peller and J. G. White, “Measurement of Ionized Calcium in Blood Platelets with a New Generation Calcium Indicator”, Biochem. Biophys. Res. Commun., 1985, 132, 652.
7) H. Ozaki, K. Sato, T. Satoh and H. Karaki, “Simultaneous Recordings of Calcium Signals and Mechanical Activity Using Fluorescent Dye Fura 2 in Isolated Strips of Vascular Smooth Muscle”, Jpn. J. Pharmacol., 1987, 45, 429.
8) M. Mitsui, A. Abe, M. Tajimi and H. Karaki, “Leakage of the Fluorescent Ca2+ Indicator Fura-2 in Smooth Muscle”, Jpn. J. Pharmacol., 1993, 61, 165.
Q&A
| Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
| A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的
有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
Fura2-AM试剂货号:F015
C44H47N3O24
1001.85
特点:
● 双波长激发检测钙离子
● 激光共聚焦,流式细胞仪均可检测
● 荧光强度高

产品性状
| 规格
性状 : 本产品为黄色或橙黄色粉末,使用时将固体溶解于无水DMSO中 纯度(HPLC): 98%以上 荧光光谱图: 符合实验要求 NMR光谱图: 符合实验要求 处理条件 保存方法 : 避光冷冻 |
产品概述
Fura 2-AM是一种可以穿透细胞膜的荧光染料。Fura 2-AM的荧光比较弱,最大激发波长为369 nm,最大发射波长为478 nm,并且其荧光不会随钙离子浓度改变而改变。Fura 2-AM进入细胞后可以被细胞内的酯酶剪切形成Fura 2,从而被滞留在细胞内。Fura 2和钙离子结合后,最大激发波长为335 nm(最大激发波长随离子浓度的的不同而有所不同),最大发射波长为505nm。实际检测时推荐使用的激发波长为340nm,发射波长为510 nm。如果做双波长检测,则推荐使用的激发波长为340 nm和380 nm。
原理
Fura 2可以和钙离子(Ca2+)结合,结合钙离子后在330-350 nm激发光下可以产生较强的荧光,而在380 nm激发光下则会导致荧光减弱。这样就可以使用340 nm和380 nm这两个荧光的比值来检测细胞内的钙离子浓度,可以消除不同细胞样品间荧光探针装载效率的差异,荧光探针的渗漏,细胞厚度差异等一些误差因素。
激发发射波长
Ex :340~380 nm
Em :510 nm
操作步骤
1、用HBSS溶液稀释1-5 mmol/l的Fura 2-AM母液,配制成1-5 μmol/l的Fura 2-AM工作液。
(此浓度仅供参考,请根据具体实验要求自行调整)
例如:1 mmol/l母液配制1 ml浓度为5 μmol/l工作液的方法:用1 ml HBSS溶液稀释5 μl母液即可。
如果Fura 2-AM进入细胞效果不好,可使用Pluronic® F-127后者可以防止Fura 2-AM在缓冲液里聚合
并能促进其进入细胞。
*Pluronic® F-127先用DMSO溶解至浓度为20%(W/V),然后根据实验需要直接加入Fura 2-AM工作液中
至终浓度为0.04-0.05%(此浓度仅供参考,请根据具体实验要求自行调整)。
2、取出预培养的细胞,除去培养基,使用HBSS溶液洗涤细胞3次。
如果使用含血清的培养基,血清中的酯酶会分解AM体,从而降低Fura 2-AM进入细胞的效果。
另外含有酚红的培养 基会使本底值略微偏高,所以加工作液之前需尽量去除培养基残留。
3、加入Fura 2-AM工作液,溶液量以覆盖细胞为准。
4、37℃细胞培养箱孵育10-60分钟,除去Fura 2-AM工作液。关于孵育的时间,
如果首次做实验不能确定,建议先孵育30分钟,看荧光效果:如果细胞死亡较多,缩短时间;
荧光强度太弱,延长时间。
5、用HBSS溶液洗涤细胞3次,以充分去除残留的Fura 2-AM工作液。然后加入HBSS溶液覆盖细胞。
6、37℃培养箱孵育约20-30分钟,以确保AM体在细胞内的完全去酯化作用。如果细胞内酯酶活性较低,
建议严格按照此操作进行;酯酶活性高的细胞实验,可以忽略此步。
7、用流式细胞仪或其它设备检测细胞,激发波长380 nm(Fura 2)和340 nm(钙离子-Fura 2)
发射波长510 nm。
注意事项
1、试剂容易吸潮,从冰箱取出后,请确认在干燥的环境放至室温后再开封。由于试剂极其微量,
开封前,请轻弹管壁几次,以保证粉末落入管底。
2、第一次使用时, 建议母液即配即用。试剂溶解后尽可能在短时间内使用,以保证实验效果。
3、溶解液DMSO需要保证新鲜无水,否则将会导致AM体水解,使荧光染料无法进入细胞,影响实验效果。
4、母液遇水极易分解,如果不能一次用完,建议分装保存,例如分装成5 μl/管,用封口膜封口,
并用铝箔纸包裹,放在一个密闭性能好的塑料袋中,并放入一包干燥剂,在≤-20℃密封避光保存。
5、建议您在正式实验前先摸索一下细胞量、钙离子荧光探针的终浓度、培养时间等,找到最佳实验条件
数据处理
Fλ1与Fλ2分别是λ1与λ2激发时的总荧光强度,Sf 1与Sf 2是两种紫外光激发时游离Fura-2 (未结合Ca2+)的荧光系数,
Cf是游离的Fura-2浓度,Sb1与Sb2是相应波长下结合Ca2+后Fura-2的荧光系数,Cb是结合Ca2+的Fura-2浓度
参考文献
1) G. Grynkiewicz, M. Poenie and R. Y. Tsien, “A New Generation of Ca2+ Indicators with Greatly Improved Fluorescence Properties”, J. Biol. Chem., 1985, 260, 3440.
2) D. A. Williams, K. E. Fogarty, R. Y. Tsien and F. S. Fay, “Calcium Gradients in Single Smooth Muscle Cells Revealed by the Digital Imaging Microscope Using Fura-2”, Nature, 1985, 318, 558.
3) R. Y. Tsien, T. J. Rink and M. Poenie, “Measurement of Cytosolic Free Ca2+ in Individual Small Cells Using Fluorescence Microscopy with Dual Excitation Wavelengths”, Cell Calcium, 1985, 6, 145.
4) D. A. Williams and F. S. Fay, “Intracellular Calibration of the Fluorescent Calcium Indicator Fura-2”, Cell Calcium, 1990, 11, 75.
5) W. Almers and E. Neher, “The Ca Signal from Fura-2 Loaded Mast Cells Depends Strongly on the Method of Dye-loading”, FEBS Lett., 1985, 192, 13.
6) G. H. R. Rao, J. D. Peller and J. G. White, “Measurement of Ionized Calcium in Blood Platelets with a New Generation Calcium Indicator”, Biochem. Biophys. Res. Commun., 1985, 132, 652.
7) H. Ozaki, K. Sato, T. Satoh and H. Karaki, “Simultaneous Recordings of Calcium Signals and Mechanical Activity Using Fluorescent Dye Fura 2 in Isolated Strips of Vascular Smooth Muscle”, Jpn. J. Pharmacol., 1987, 45, 429.
8) M. Mitsui, A. Abe, M. Tajimi and H. Karaki, “Leakage of the Fluorescent Ca2+ Indicator Fura-2 in Smooth Muscle”, Jpn. J. Pharmacol., 1993, 61, 165.
Q&A
| Q1: 细胞内检测钙离子的试剂种类都有什么,选择什么样的比较好呢? |
| A1: 根据检测仪器和检测波长有很多的选择,产品后面标有AM的试剂是可以通过细胞膜的
有很多种相似的试剂,其特点如下: 【Fura 2】 •双波长激发 激发(λex= Ca:340 nm, Ca free:380 nm)、发射:λem=500 nm •解离常数:224 nmol/L •因为是荧光强度的比值、可以有效的减小误差 =>細胞内Ca浓度计算。 •该试剂被使用的最多 •必须要更换过滤片、会耽误一些时间。 【Fluo 3】 •单波长激发 激发:λex=508 nm、发射:λem=527 nm •解离常数:400 nmol/L •因为激发光在长波段,所以对细胞的损伤比较小 (不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •不适合切片中钙离子的检测 •【Fluo 4】 •单波长激发 •激发:λex=495 nm、发射:λem=518 nm •解离常数:360 nmol/L •与Fluo3相比对荧光强度更高。 •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •与Fluo3相比对細胞的毒性低 •【Indo 1】 •单波长激发 •激发:λex= 330 nm、发射(λem= Ca:410 nm, Ca free:485 nm) •解离常数:250 nmol/L •由于不需要更换滤光片,可以很快地检测细胞内钙离子浓度变化以及像心肌细胞运动中钙离子的变化 •(需要两台检测仪器) •【Rhod 2】 •单波长激发 •激发:λex=553 nm、发射:λem=576 nm •解离常数:1.0 μmol/L •因为激发光在长波段,所以对细胞的损伤比较小 •(不会受到NADH、NADPH的影响) •可以使用Ar激光激发装置。 •【Quin 2】 •单波长激发 •激发:λex=339 nm、发射:λem=492 nm •解离常数:110 nmol/L •最早开发的产品 |
荧光探针,Dojindo同仁化学
各种钙离子探针参数对比
| 产品名称 | Quin 2 | Fura 2-AM | Fluo 3-AM | Rhod 2-AM | Fluo 4-AM |
| 激发波长 | 339 nm | 340 nm/380 nm | 508 nm | 553 nm | 495 nm |
| 发射波长 | 492 nm | 510 nm | 527 nm | 576 nm | 518 nm |
| 解离系数 | 115 nmol/l | 224 nmol/l | 0.4 umol/l | 1.0 umol/l | 345 nmol/l |
| 产品特点 | 早起研发钙定量 | 可定量钙离子 | 绿色荧光探针 | 红色荧光探针 | 高强度荧光探针 |
BAPTA-AM试剂货号:B018
C34H40N2O18
764.68
特点:
● 螯合率高于EGTA
● 可螯合细胞内的钙离子
性质
BAPTA-AM是BAPTA羧基的乙酰氧基甲基酯化产物,可以很容易地吸收到细胞中。 该酯被细胞内酯酶分解,显示出主体在细胞中作为BAPTA的功能。 生成的BAPTA保留在细胞内部。
参考文献
1) R. Y. Tsien, “New Calcium Indicators and Buffers with High Selectivity against Magnesium and Protons: Design, Synthesis, and Properties of Prototype Structures”, Biochemistry, 1980, 19 (11), 2396.
2) R. Y. Tsien, “A Non-disruptive Technique for Loading Calcium Buffers and Indicators into Cells”, Nature, 1981, 290, 527.
3) J. I. Korenbrot, D. L. Ochs, J. A. Williams, D. L. Miller and J. E. Brown, “The Use of Tetracarboxylate Fluorescent Indicators in the Measurement and Control of Intracellular Free Calcium Ions”, Soc. Gen. Physiol. Ser., 1986, 40, 347.
4) S. M. Harrison and D. M. Bers, “The Effect of Temperature and Ionic Strength on the Apparent Ca-affinity of EGTA and the Analogous Ca-chelators BAPTA and Dibromo-BAPTA”, Biochim. Biophys. Acta, 1987, 925, 133.
5) E. W. Gelfand and R. K. Cheung, “Dissociation of Unidirectional Influx of External Ca2+ and Release from Internal Stores in Activated Human T Lymphocytes”, Eur. J. Immunol., 1990, 20, 1237.
6) J. P. Kao, J. M. Alderton, R. Y. Tsien and R. A. Steinhardt, “Active Involvement of Ca2+ in Mitotic Progression of Swiss 3T3 Fibroblasts”, J. Cell Biol., 1990, 111, 183.
7) M. L. Schubert and J. Hightower, “Functionally Distinct Muscarinic Receptors on Gastric Somatostatin Cells”, Am. J. Physiol., 1990, 258, G982.
8) Y. Tojyo and Y. Matsumoto, “Inhibitory Effects of Loading with the Calcium-chelator 1, 2-Bis(o-aminophenoxy)ethane-N,N,N’,N’-tetraacetic acid (BAPTA) on Amylase Release and Cellular ATP Level in Rat Parotid Cells”, Biochem. Pharmacol., 1990, 39(11), 1775.
规格性状
规格性状:
该产品为无色液体。
纯度(HPLC):98.0%以上
处理条件
1.危险物第4类,第3石油类,危险等级Ⅲ 2.无火 3.储存方法:冷冻,避光
组织染色,溶酶体,细胞染色,Dojindo同仁化学
| 染料名 | 检测法 | 荧光色 | λex (nm) | λem (nm) | 染色参考 |
| BCECF-AM | 荧光 | 绿 | 490 | 526 | 进入细胞内AM体分解 |
| Calcein-AM | 荧光 | 绿 | 490 | 515 | 进入细胞内AM体分解 |
| CFSE | 荧光 | 绿 | 496 | 516 | 结合细胞内的蛋白质 |
| FDA | 荧光 | 绿 | 488 | 530 | 細胞内加水分解 |
| PI | 荧光 | 红 | 530 | 620 | 只能染色死細胞(蓝色) |
| AO | 荧光 | 绿 | 502 | 526 | 细胞核染色 |
| DAPI | 荧光 | 兰 | 360 | 460 | 结合死细胞的核酸 |
| Hoechst 33258 | 荧光 | 兰 | 350 | 461 | 结合活细胞/死细胞核酸 |
| Hoechst 33342 | 荧光 | 兰 | 352 | 461 | 结合死细胞的核酸 |
| MitoRed | 荧光 | 红 | 560 | 580 | |
| Rh123 | 荧光 | 绿 | 507 | 529 | |
| MitoBright LT Green | 荧光 | 绿 | 493 | 508 | 线粒体染色 |
| MitoBright LT Red | 荧光 | 红 | 548 | 564 | 线粒体染色 |
| MitoBright LT Deep Red | 荧光 | 深红 | 644 | 666 | 线粒体染色 |
| 染料名 | 检测法 | 荧光色 | λex (nm) | λem (nm) | 染色参考 |
| BCECF-AM | 荧光 | 绿 | 490 | 526 | 进入细胞内AM体分解 |
| Calcein-AM | 荧光 | 绿 | 490 | 515 | 进入细胞内AM体分解 |
| CFSE | 荧光 | 绿 | 496 | 516 | 结合细胞内的蛋白质 |
| FDA | 荧光 | 绿 | 488 | 530 | 細胞内加水分解 |
| PI | 荧光 | 红 | 530 | 620 | 只能染色死細胞(蓝色) |
| AO | 荧光 | 绿 | 502 | 526 | 细胞核染色 |
| DAPI | 荧光 | 兰 | 360 | 460 | 结合死细胞的核酸 |
| Hoechst 33258 | 荧光 | 兰 | 350 | 461 | 结合活细胞/死细胞核酸 |
| Hoechst 33342 | 荧光 | 兰 | 352 | 461 | 结合死细胞的核酸 |
| MitoRed | 荧光 | 红 | 560 | 580 | |
| Rh123 | 荧光 | 绿 | 507 | 529 | |
| MitoBright LT Green | 荧光 | 绿 | 493 | 508 | 线粒体染色 |
| MitoBright LT Red | 荧光 | 红 | 548 | 564 | 线粒体染色 |
| MitoBright LT Deep Red | 荧光 | 深红 | 644 | 666 | 线粒体染色 |
细胞染色
β-淀粉样物质,细胞染色,Dojindo同仁化学
| 染料名 | 检测法 | 荧光色 | λex (nm) | λem (nm) | 染色参考 |
| BCECF-AM | 荧光 | 绿 | 490 | 526 | 进入细胞内AM体分解 |
| Calcein-AM | 荧光 | 绿 | 490 | 515 | 进入细胞内AM体分解 |
| CFSE | 荧光 | 绿 | 496 | 516 | 结合细胞内的蛋白质 |
| FDA | 荧光 | 绿 | 488 | 530 | 細胞内加水分解 |
| PI | 荧光 | 红 | 530 | 620 | 只能染色死細胞(蓝色) |
| AO | 荧光 | 绿 | 502 | 526 | 细胞核染色 |
| DAPI | 荧光 | 兰 | 360 | 460 | 结合死细胞的核酸 |
| Hoechst 33258 | 荧光 | 兰 | 350 | 461 | 结合活细胞/死细胞核酸 |
| Hoechst 33342 | 荧光 | 兰 | 352 | 461 | 结合死细胞的核酸 |
| MitoRed | 荧光 | 红 | 560 | 580 | |
| Rh123 | 荧光 | 绿 | 507 | 529 | |
| MitoBright LT Green | 荧光 | 绿 | 493 | 508 | 线粒体染色 |
| MitoBright LT Red | 荧光 | 红 | 548 | 564 | 线粒体染色 |
| MitoBright LT Deep Red | 荧光 | 深红 | 644 | 666 | 线粒体染色
|
细胞染色
BCECF-AM试剂货号:B262
C35H28O15
688.59
特点:
● 水溶性好,可进入细胞膜
● 荧光强度高

凑单关联产品TOP5
NO.1. Annexin V, FITC Apoptosis Detection Kit 细胞凋亡检测
NO.2. Cell Counting Kit-8 细胞增殖毒性检测
NO.3. Cytotoxicity LDH Assay Kit-WST 乳酸脱氢酶(LDH)检测
NO.4. Cell Viability Assay Kit 细胞增殖/毒性检测
NO.5. Fluo 4-AM special packaging 细胞内钙离子检测
规格性状
规格
特性:该产物为浅橙色至浅橙色棕色粉末或固体,可溶于DMSO和乙腈。
纯度(HPLC):90%以上
荧光光谱:试验成功
NMR光谱:试验成功
产品概述
BCECF被广泛地用于细胞内pH的测定。Tsien博士和其他人通过加入2个额外的羧化物基团改进了这种羧基荧光素。加入的两个羧基使得它能更好地被固定在细胞内。BCECF具有很好的水溶性,是因为它在中性pH时带有4-5个负电荷。但是BCECF却很难穿过细胞膜进入到细胞内。它的pKa值为6.97,高于其它的羧基荧光素。BCECF在激发光谱439nm处有等吸收点,因此它能和Fura 2一样可用比率法测定。505nm和439nm通常是非常有用的用于比率测量的波长,一般会将490nm和450nm的滤光片加在激发光源的前面。而530nm的滤光片则是用来查看它的荧光信号的。这里要注意的是激发光谱与吸收光谱有一些细微的区别。BCECF-AM是乙酰甲酯化的BCECF。它能够轻易地进入到细胞内。就和其他的乙酰甲酯类一样,BCECF-AM只需要通过孵育就能进入细胞。BCECF-AM对潮湿非常敏感,所以要小心保存。如果DMSO储存液的颜色从浅黄色变为深橙色就代表了AM的分解。所以通过对颜色变化的观测,能判断AM酯的水解情况。

产品特性
BCECF-AM是一种对细胞内pH敏感的新型荧光探针,分别用490nm和440nm波长激发BCECF所得到的发射荧光之比与pH有很好的线性关系。BCECF-AM是乙酰甲酯化的BCECF,BCECF-AM是一种可以穿透细胞膜的荧光染料,BCECF-AM没有荧光,进入细胞后被细胞内的酯酶水解成BCECF,从而被留在细胞内。BCECF在适当的pH值情况下可以被激发形成绿色荧光。BCECF-AM不仅被广泛用于哺乳动物细胞的研究,也有报道用于动物组织、植物细胞、细菌和酵母等的细胞内pH水平检测。在有细胞内pH变化的细胞毒性、细胞凋亡、细胞粘附、药物抵抗、细胞趋化等过程中BCECF AM被广泛应用。BCECF-AM(pH荧光探针)需用无水DMSO(anhydrous DMSO)配制。

操作说明
试剂 (溶解方法):
1.45 mM的BCECF-AM/DMSO溶液(将1 mg 的BCECF-AM溶于1mlDMSO)HEPES缓冲液(20mM HEPES,153mM NaCl,5mM KCl,5mM glucose,pH7.4)
操作:
1.用HEPES制备细胞悬液,细胞浓度为4×107个/ml。
2.将1.45 mM的BCECF-AM/DMSO溶液加入细胞悬液中 (细胞悬液的1/300体积),BCECF-AM终浓度为3mM。
3.37℃培养30min。
4.用HEPES缓冲液清洗细胞3次,制成3×106个/ml的细胞悬液。
5.使用荧光显微镜或带有图像分析系统的激光共聚焦显微镜检测细胞的荧光强度。
*标记的条件因细胞种类而异,在每次实验前,请先确定最佳条件。以上方法仅供参考。

活细胞质染色-绿色——Calcein-AM货号:C326
C46H46N2O23
994.86
特点:
● 活细胞和死细胞可同时染色
● 490 nm激发波长,515 nm发射波长

活动进行中
订购满5000元,200元礼品等你拿
凑单关联产品TOP5
NO.1. Cell Counting Kit-8 细胞增殖毒性检测
NO.2. Cytotoxicity LDH Assay Kit-WST 乳酸脱氢酶(LDH)检测
NO.3. FerroOrange 细胞亚铁离子检测
NO.4. Cellstain- PI 细胞核染色
NO.5. Annexin V, FITC Apoptosis Detection Kit 细胞凋亡检测
规格性状
规格
特性:该产物为无色至微黄色固体,可溶于二甲基亚砜和乙腈。
可溶于二甲基亚砜:试验成功
NMR光谱:试验成功
产品概述
Calcein-AM是一种可对活细胞进行荧光标记的细胞染色试剂,由于它在Calcein的基础上加强了疏水性,因此能够轻易穿透活细胞膜。当其进入到细胞质后,酯酶会将其水解为Calcein留在细胞内,发出强绿色荧光。与其它同类试剂 (如BCECF-AM和Carboxy-fluorescein diacetate) 相比,Calcein-AM是最适合作为荧光探针去染活细胞的,因为它的细胞毒性很低。Calcein不会抑制任何的细胞功能如增殖或淋巴球的趋化性。使用了Calcein的活性检测的实验结果是十分可信并且与标准的51Cr-释放法所得结果相一致的。Calcein的激发和发射波长分别为490nm和515nm。
Calcein-AM可与PI结合使用,分别对活细胞和死细胞染色,可用于同时对活细胞和死细胞进行荧光染色。
*Caution*
Please tap the tube before opening, and open it with care. The content may have relocated from the bottom of the tube during the shipping.
*警告*
打开前请先轻敲试管,并小心打开。 在运输过程中,内装物可能已从试管底部移开。

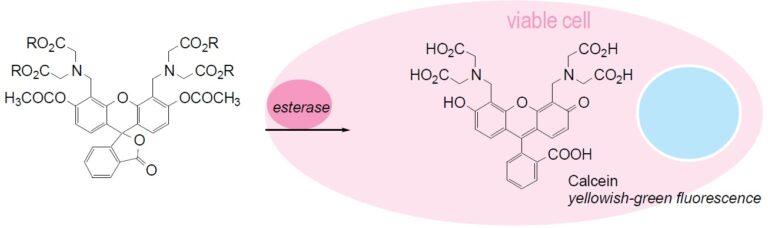
原理
Fig. 1 Cell staining mechanism
产品特性
钙黄绿素-AM通过钙黄绿素的四个羧基的乙酰氧基甲基酯化(AM转化)而使其可透过细胞膜。钙黄绿素-AM本身几乎不显示荧光,但通过细胞内酯酶水解变成钙黄绿素。该钙黄绿素是不透膜的化合物,表现出强的黄绿色荧光(λex= 490 nm,λem= 515 nm)。羧基荧光素二乙酸盐(CFDA)和荧光素二乙酸盐(FDA)与荧光素-AM具有相同的荧光素骨架,被称为染色活细胞的染料。但是,这些化合物在显色后容易从细胞膜泄漏,这已成为使用中的问题之一。与这些染料相比,钙黄绿素-AM越来越多地用作显色后从细胞泄漏较少的染料。还已知它不抑制细胞功能,例如淋巴细胞增殖和白细胞趋化性。另外,钙黄绿素-AM在利用杀伤性T细胞和NK细胞的细胞毒性活性的测定中,与使用广泛使用的放射性同位素的51Cr释放方法得到相同的结果,因此细胞毒性较小。钙黄绿素-AM对活细胞染色,并用于在荧光显微镜和流式细胞仪下观察,但是当与死细胞染色染料组合使用时,常用于活细胞和死细胞的双重荧光染色。Papadopoulus等人使用Calcein-AM和Ethidium homodimer(EthD-1)进行双重染色,并使用两种染料的荧光波长差异通过流式细胞术研究细胞毒性。钙黄绿素-AM目前是用于染色活细胞的最有用的染料,因为它的细胞毒性较小,荧光后细胞泄漏较少。如上所述,目前正在使用放射性同位素的测量方法,但是从安全性和便利性的角度出发,期望使用荧光化合物的细胞研究的分析将继续进行。
荧光特性
λex=490 nm, λem=515 nm
操作说明
1. 用1ml无水DMSO溶解1 mg Calcein-AM,制备成1 mmol/l的Calcein-AM母液,-20℃下密闭冷冻保存。
2. 用PBS将Calcein-AM母液稀释制成1-50 µM的Calcein-AM溶液(现配现用)。
3. 吸掉预培养好的细胞中的培养基,用合适的缓冲液清洗2-3次。a)
4. 加入适量的Calcein-AM溶液,在37℃培养细胞15-30分钟。
5. 用PBS或适当的缓冲液洗涤细胞两次。
6. 用490 nm激发波长,515 nm发射波长的滤光片的荧光显微镜观察细胞。
a) 如果Calcein-AM很难进入细胞,可以使用表面活性剂,如Pluronic® F127。
参考文献
1) K. McGinnes, G.Chapman, R.Marks and R.Penny, “A Fluorescence NK Assay Using Flow Cytometry”, J.Immunol.Methods,1986,86,7.
2) S.J.Morris,”Real-time Multi-wavelength Fluorescence Imaging of Living Cells”, BioTechniques,1990,8(3),296.
3) S.A.Weston and C.R.Parish,”New Fluorescent Dyes for Lymphocyte Migration Studies Analysis by Flow Cytometry and Fluorescent Microscopy”, J.Immunol.Methods,1990,133,87.
4) D.M.Callewaert,G.Radcliff,R.Waite,J.Lefevre and D.Poulik,”Characterization of Effector-Target Conjugates for Cloned Human Natural Killer and Human Lymphokine Activated Killer Cells by Flow Cytometry”,Cytometry,1991,12,666.
5) Han-Qing Xie, R.Huang and V.W.Hu, “Intercellular Communication Through Gap Junctions Is Reduced in Senescent Cell”, Biophys.J,1992,62,45.
6) S.A.Weston and C.R.Parish,”Calcein: a Novel Marker for Lymphocytes Which Enter Lymph Nodes”,Cytometry,1992,13,739.
7) X.M.Wang, P.I.Terasaki,G.W. Rankin Jr. ,D.Chia,H.P.Zhong and S.Hardy,”A New Microcellular Cytotoxicity Test Based on Calcein AM Release”, Hum. Immunol.,1993,37,264.
8) N.G.Papadopoulos,G.V.Dedoussis,G.Spanakos,A.D.Gritzapis, C.N.Baxevanis and M.Papamichail,”An Improved Fluorescence Assay for the Determination of Lymphocyte-Mediated Cytotoxicity Using Flow Cytometry”, J.Immunol.Methods,1994,177,101.
9) L.S.De Clerck,C.H.Bridts,A.M.Mertens,M.M.Moens and W.J.Stevens,”Use of Fluorescent Dyes in the Determination of Adherence of Human Leucocytes to Endothelial Cells and the Effects of Fluorochromes on Cellular Function”, J.Immunol. Methods,1994,172,115.
10) H.Ohata,Y.Ujiki and K.Momose,”Confocal Imaging Analysis of ATP-Induced Ca2+ Response in Individual Endothelial Cells of the Artery in Situ”, Am.J.Physiol. ,1997,272(6),1980.
常见问题Q&A
| Q1:与51Cr释放方法有关吗 |
|
A1: “钙黄绿素-AM与51Cr释放方法之间存在相关性。 以下文件中有一份报告。N.G.Papadopoulos, et.al., J.Immunol.Methods, 177,101-111(1994)” |
|
Q2:细胞染料的激发波长和发射波长是多少。 |
| A2: |
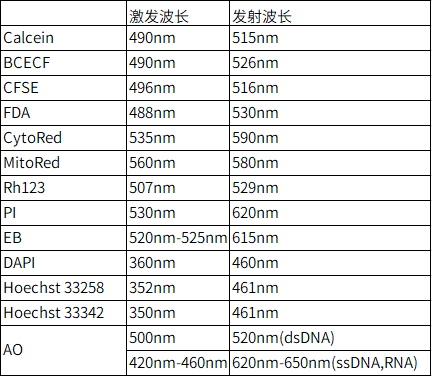
|
Q3:细胞染色试剂Cellstain的哪些活细胞染色染料可以在细胞中长时间停留? |
|
A3: “就细胞内保留而言,“ CFSE”可以在细胞中停留最长时间。尽管荧光强度降低,但是已经证实细胞中存在荧光染料达8周。用“ Calcein-AM”和“ BCECF-AM”观察到荧光达3天。也有报道称“钙蛋白-AM”在6小时内在细胞中保留了90%” ・S.A.Weston, et.al., J.Immunol.Methods, 133, 87-97(1990) ・H.P.Zhong, et.al., Hum.Immunol., 37, 264-270(1993)” 但是,“钙调蛋白-AM”和“ BCECF-AM”对细胞毒活性没有影响。 ・L.S.D.Clerck, et.al., J.Immunol.Methods, 172, 115-124(1994) 还要注意的一点是,原始的基本骨架是荧光素,因此由于激发光而褪色由于容易发生,因此可能难以通过长期激发来观察荧光。 (尽管最好使用防褪色剂等) |
| Q4:如何使用Calcein-AM。 |
|
A4:下面以HeLa细胞的情况为例进行介绍。 根据细胞类型和观察条件考虑并固定试剂浓度。 【试剂】 溶液A:将1 mg钙黄绿素-AM溶于1 ml DMSO→1 mmol / L溶液 *将溶液存放在-20°C的阴凉处,以防止变质。 溶液B:用PBS(-)将溶液A稀释500倍(用5 mL PBS稀释10μl溶液A得到2μmol/ L)。 * Calcein-AM在水溶液中分解,因此在使用前请准备溶液B。 【操作】 1)用胰蛋白酶-EDTA收集HeLa细胞并制备细胞悬液。 2)离心细胞悬液(1,000 rpm,3分钟) 3)除去上清液并添加PBS(-)(此时,准备细胞数为105至106细胞/ mL)。 4)用移液器充分分散。 *由于培养液中的血清可能会升高背景,请执行操作2)至4)。 重复并彻底清洗。 5)将30μl在4)中获得的细胞悬液添加至1.5ml微管中。 6)向其中加入15μL[液体B]。 7)盖上微管并在37°C下孵育15分钟。 8)将10μL7)的溶液放在盖玻片上,从上方堆叠盖玻片,然后将染色的细胞悬液夹在中间。 9)将盖玻片放在荧光显微镜下,用490 nm的滤光片激发,观察发出黄绿色荧光的活细胞。 (对于滤光片,如果是490±10 nm,则可以观察到) *排除血清和酚红,因为它们是背景。 *如果背景很高,请清洁它。 *在载玻片上培养的细胞可以用相同的方式染色和观察。 *有关使用PI的双重染色方法,请参阅方案“我要分别对活细胞和死细胞进行染色”。 |
|
Q5:我已经购买了钙黄绿素-AM(粉末),并希望将其制成溶液。 我该怎么办? |
|
A5:溶于DMSO。 分子量几乎为1000,因此,如果将1 mg溶于1 mL DMSO,它将是1 mM的溶液。 请使用尽可能干燥的DMSO。 |

